服务搜索 SEARCH

|
中国医疗器械注册
TECERT提供一站式中国医疗器械产品注册咨询服务。
医疗器械产品的分类:
依据《医疗器械分类规则》(国家局令第15号)和《医疗器械分类目录》(国药监械[2002]302号),我国将医疗器械共分为三大类:
第一类是指通过常规管理足以保证安全性、有效性的。
第二类是指产品机理已取得国际国内认可,技术成熟,安全性、有效性必须加以控制的。
第三类是指植入人体,或用于生命支持,或技术结构复杂,对人体可能具有潜在危险安全性、有效性必须加以严格控制的。
医疗器械产品的注册:
所有医疗器械产品在正式投产前,都要先获得(中国)国家食品药品监督管理局(英文简称SFDA)的注册认证。注册的目的是依照法定程序,对拟生产、上市销售、使用的医疗器械的安全性、有效性进行系统评价,以决定是否同意其销售、使用的过程4。在临床实验完成的前提下,整个注册过程需要2-3个月的时间。
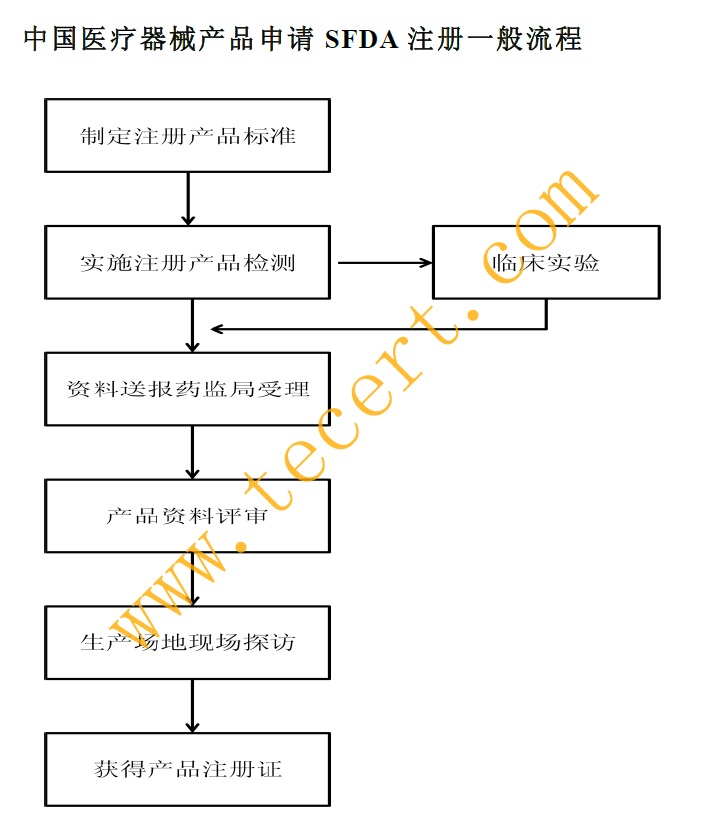
中国医疗器械产品申请SFDA注册一般流程: